皆さんはカゼインの等電点がpH 4.6であり、乳のpHをさげていくと等電点で沈殿あるいは凝固することをよくご存じだと思います。しかし、何故等電点で沈殿するのか、ホエイたんぱく質はその等電点(pH 5.2付近)でどうなるか説明できる方は少ないのではないかと思います。たんぱく質は等電点で沈殿するものと考えている方も多いのではないでしょうか。
たんぱく質はアミノ酸が多数つながったものですが、アミノ酸には中性にてマイナスのもの(グルタミン酸、アスパラギン酸)、プラスのもの(リジン、アルギニン、ヒスチジン)、疎水性を示すもの(フェニルアラニン、チロシン、ロイシン、イソロイシン、バリン、トリプトファン)、水に親和的なOH基を持つもの(セリン、トレオニン)、その他があります。
しかし、アミノ酸の電荷はpHで変わります。グルタミン酸やアスパラギン酸はpHが酸性になるとCOO- がCOOHとなり電荷を失います。一方、プラスの電荷を持つアミノ酸は中性からアルカリ性になるとNH3+がNH2となり、プラスの電荷を失います。カゼインの場合はpH 4.6になるとマイナス電荷の数とプラス電荷の数が等しくなり、カゼイントータルでは電荷がゼロになります。なので、pH 4.6が等電点なのです。
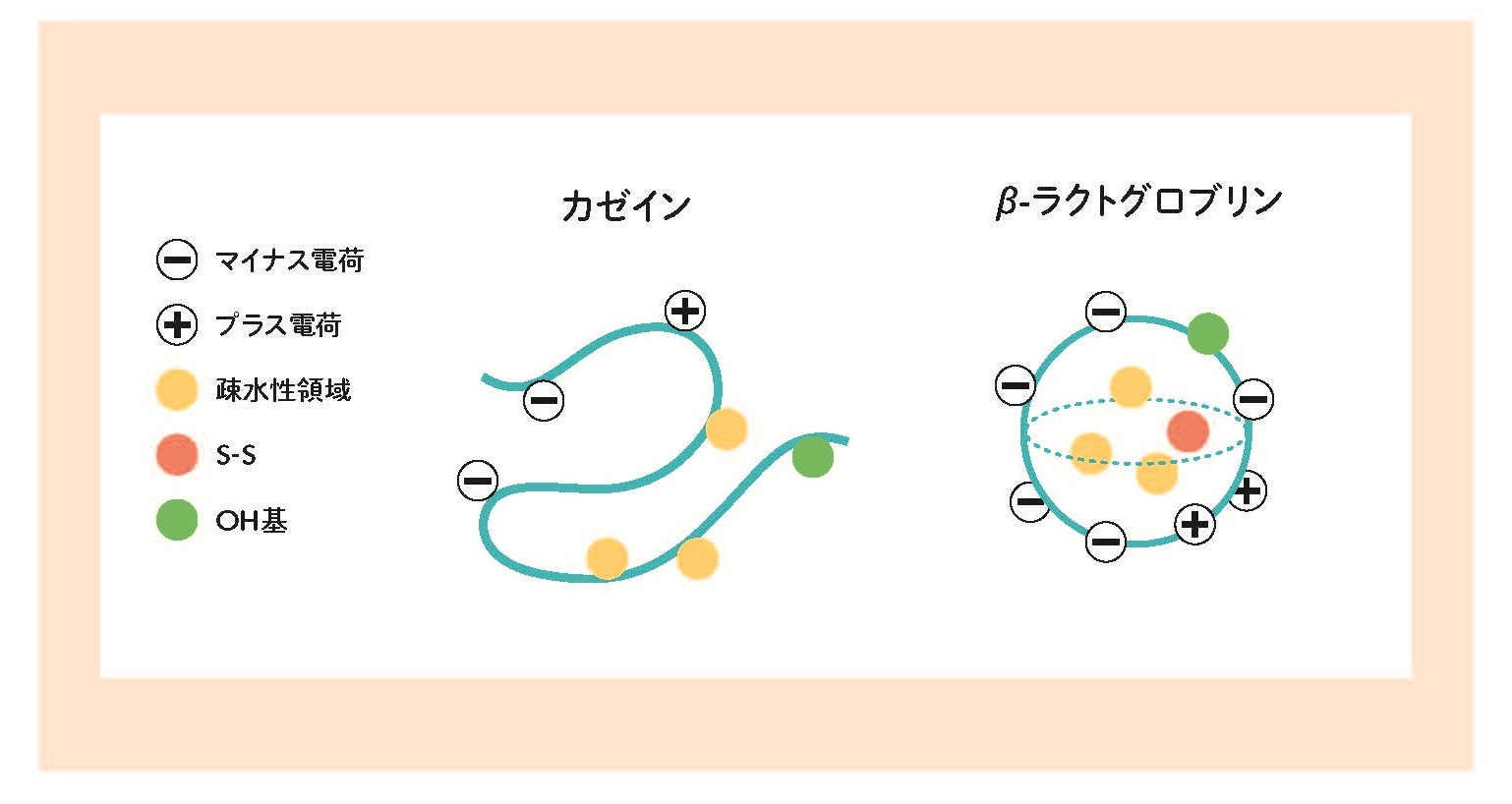
さて、たんぱく質が沈殿するかしないかはたんぱく質粒子が大きいか小さいかで決まります。カゼインの場合は等電点にてカゼインが凝集し大きくなります。なので、沈殿するのです。もし凝集しなければ沈殿しません。たんぱく質の粒子が互いに凝集する要因は、疎水性相互作用とS-S結合です。S-S結合はシステイン(CysSH)同士が加熱によりシスチン(CysS-SCys)となる結合です。二つ目は疎水性相互作用です。これは疎水性アミノ酸が水との接触を避けるために、たんぱく質の疎水性領域どうしが凝集する現象です。一方、疎水性相互作用に対して、水との親和性が高い領域は電荷のあるアミノ酸とOH基(セリン、トレオニン、糖鎖)です。
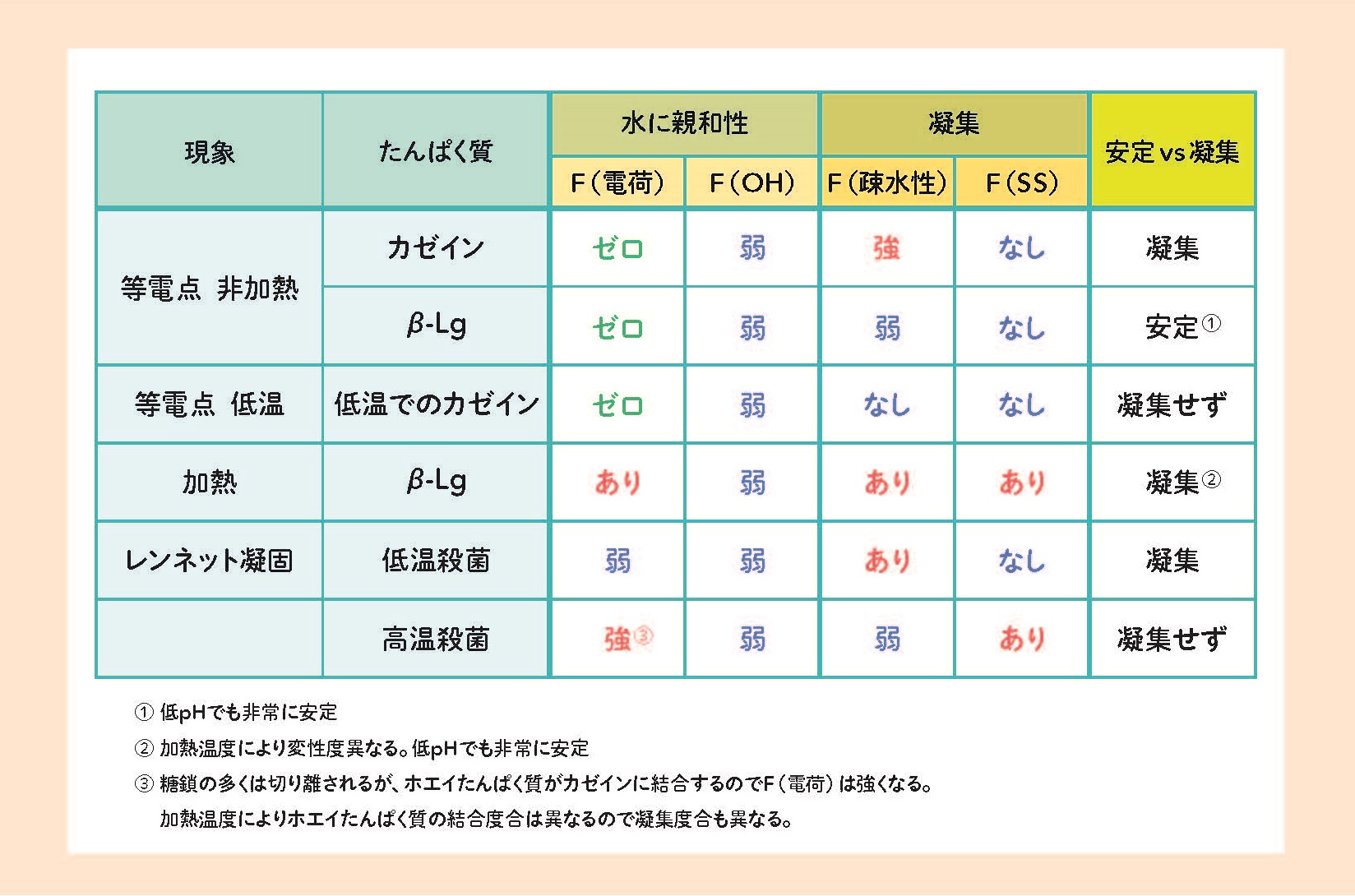
このようにたんぱく質は水に親しい勢力の大きさF(電荷)とF(OH)、水を避ける勢力の大きさF(疎水性)とS-S結合によりたんぱく質どうしが凝集する勢力F(SS)が働いており、F(電荷) + F(OH) とF(疎水性) + F(SS)の大小で、凝集するか、凝集しないかが決まります。カゼインの場合はシステインが殆ど含まれていないのでF(SS)がなく、等電点ではF(電荷)もゼロですから、F(OH)とF(疎水性)の大小関係を考えればよいわけです。
しかし、牛乳の温度が低温(2~3℃)になると、F(疎水性)は働きません。その場合、OH基による弱い勢力のみが働きますので、カゼインは沈殿しません。その理由は熱力学の法則から導かれるのですが、難しいのでここでは説明を省きます(詳しくは、『乳・乳製品の知識』堂迫俊一、幸書房参照)。
一方、ホエイたんぱく質の主要たんぱく質であるβ-ラクトグロブリン(β-Lg)は加熱されていない生の状態では等電点(pH 5.2)になっても沈殿しません。これは球状たんぱく質であるβ-Lgの疎水性アミノ酸は粒子の内側に埋もれており、表面は電荷を持つアミノ酸とOH基を持つアミノ酸がメインとなっています。なので、等電点にてF(電荷)がゼロとなってもF(OH)の働きで沈殿しないのです。しかし、加熱すると粒子の立体構造がほどけて(変性)疎水性アミノ酸が粒子の表面に露出してきます。加熱温度によって変性の程度が異なり、大きく変性しF(疎水性)が大きければ沈殿するし、変性が少なければ沈殿しません。リコッタを作る場合は十分加熱して変性させることが歩留向上につながります。また、少量の牛乳をホエイに添加することが一般的ですが、加熱変性したホエイたんぱく質とカゼインが会合すれば等電点付近ではカゼイン+ホエイたんぱく質のF(電荷)はほぼゼロになり、F(疎水性)のみが働くのでリコッタの歩留が高くなります。
牛乳の加熱殺菌温度がいわゆる低温殺菌の場合にはレンネット凝固や乳酸菌発酵でカゼインが凝固し、ホエイたんぱく質が残ります。しかし、高温殺菌した乳ではカゼインがしっかり凝固しません。何故でしょう。高温殺菌によりホエイたんぱく質が加熱変性し、S-S結合や疎水性相互作用によりカゼインに結合します。するとカゼイン+ホエイたんぱく質の表面電荷は増え、疎水性アミノ酸やSH基は減少します。つまり、F(電荷)+F(OH)がF(疎水性)+F(SS)より高くなります。レンネットを作用させ糖鎖(OH基)を含むκ-カゼインマクロペプチド(GMPともいう)が遊離するとF(OH)が低下しますが、ホエイたんぱく質がカゼインに会合するのでF(電荷)が増えます。そのため、沈殿しにくい、もしくは沈殿しても十分な凝固カードになりにくいのです。
このように、チーズを作る、あるいは料理などに利用する場合、カゼインの電荷や疎水性がどうなっているかを考えてみると役に立つと思います。
「乳科学 マルド博士のミルク語り」は毎月20日に更新しています。
ⒸNPO法人チーズプロフェッショナル協会
無断転載禁止