技術革新はしばしば失敗、偶然、あるいは常識を覆す発想から生み出されることがあります。例えば16世紀、コペルニクスは天体観察をしていたら、それまでは常識だった天動説では説明できない天体現象から地動説を唱えたことは皆様もご存じのとおりです。ニュートンは木からりんごが落ちるのを見て万有引力を発見したと伝えられています。実際には「木からりんごが落ちるのに、月は落ちてこないのは何故か」を考え、「月も落ちてくるが遠心力が働いているので落ちてこない」と考えたのが真相のようです。
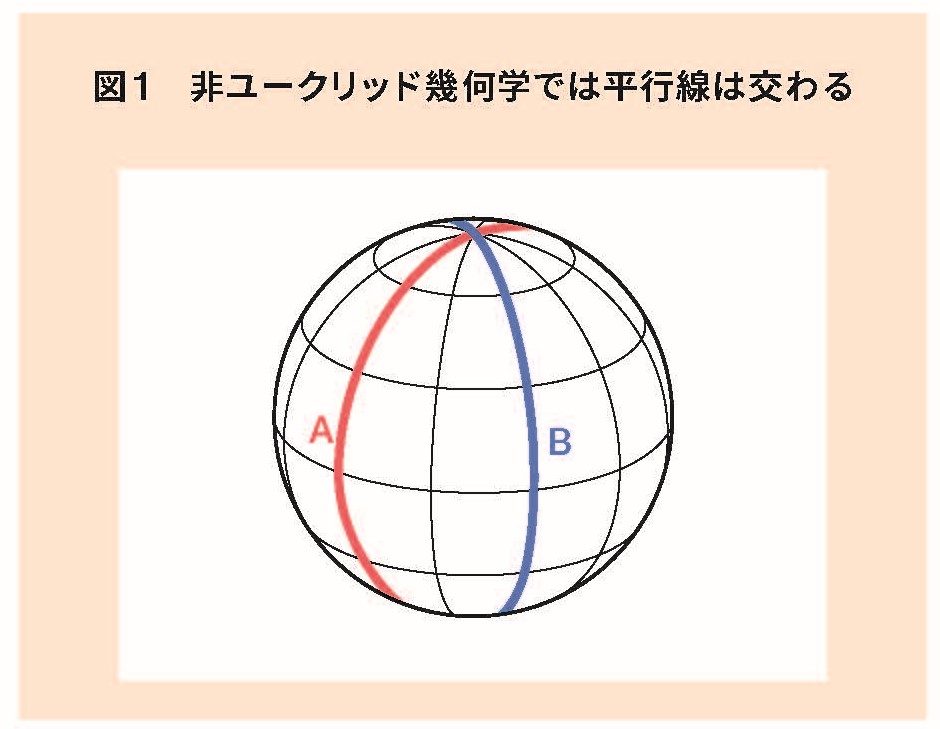
私たちは学校で”平行線は交わらない”と習いました、これがユークリッド幾何学で、数学の入試問題には必ず1問はユークリッド幾何学に基づいた図形問題が出題されています。しかし、”平行線は交わる”も正しいのです。地球の赤道に直角となるように平行線(経線)を引くと、北極や南極でこの経線は交わります(図1)。なので、平行線は交わるのです。これが非ユークリッド幾何学の基本です。
先日、TVを観ていたら、今日に至るまで未完成のサグラダファミリアにて彫刻を担当している外尾悦郎氏が、ガウディの設計図などない彫刻の復元について、常識に囚われていてはダメだ、常識に囚われない発想が必要だ、といった趣旨の話をされていました。
生化学系の研究者はたんぱく質の性質を調べる際、そのたんぱく質を緩衝液に溶かして実験に供します。緩衝液とはある特定のpH範囲ではpHの変化が少ない溶液で、一般的にはリン酸緩衝液(中性付近で使われます)、クエン酸緩衝液(弱酸性付近で使用)、トリス緩衝液(トリスヒドロキシメチルアミノメタン、弱アルカリ性付近で使用)などが知られています。何故、これらを使うかというと、生体内のpHに近いため、生体内でのたんぱく質の性質を調べやすいためです。そのため緩衝液に溶かして実験することが常識で目的に応じた緩衝液を選びます。
しかし、食品としてカゼインの性質を調べたり、製造技術を開発したりする場合はどうでしょうか。カゼインが体内で消化酵素によりどのように分解されるかを調べる場合、胃での反応を調べるには酸性領域に適した緩衝液を使うことが勧められます。小腸での反応を調べるには中性領域に適した緩衝液、多くはリン酸緩衝液が使われます。ところが、多くの場合カゼインミセルにはカルシウムが結合しています。胃の中で一旦カルシウムは外れますが、小腸で再びカゼインとカルシウムが混在した状態になります(カルシウムが先に小腸に到達し、カゼインは後着するのかも)。リン酸緩衝液を使うとカルシウムはリン酸カルシウムとなり、カゼインとリン酸カルシウムが混在する状態となるので、体内とは異なる可能性があります。また、熟成中のチーズに働く酵素や生じるペプチドなどの挙動を調べる場合も、緩衝液を使うことが適しているのか、使うならどの緩衝液が適切かなど充分に考えて計画する必要があります。
筆者は昔、ラクトフェリンの研究に携わっていた時期がありましたが、馬鹿の一つ覚えで、リン酸緩衝液に溶かして耐熱性を調べていました。ラクトフェリンは耐熱性が低く、65℃を超えると沈殿します。ある時、たんぱく質に詳しくない方から、ラクトフェリンを使いたいと言われ、渡しました。そしたら、彼はラクトフェリンを鍋に入れて水道水を加え、ガスコンロに載せて加熱し始めました。筆者はびっくりし、慌てました。しかし、ラクトフェリンは沈殿しなかったのです。そこで、常識を捨てて、詳しく調べたらイオン強度とpHを調整すると加熱しても沈殿しないことが分かり、加熱殺菌方法を開発できました。
先日ある乳業メーカーが牛乳を急速冷凍して販売することを始めたというニュースを読みました。牛乳を凍結すると食感が悪くなるというのが常識でした。それを覆し急速冷凍するという考え方はすばらしいアイディアだと思います。但し、価格が高いこと、牛乳の冷凍輸送、販売店での冷凍販売への対応などが必要なことから全国展開するにはまだまだ時間がかかると考えます。今後の展開が期待されます。
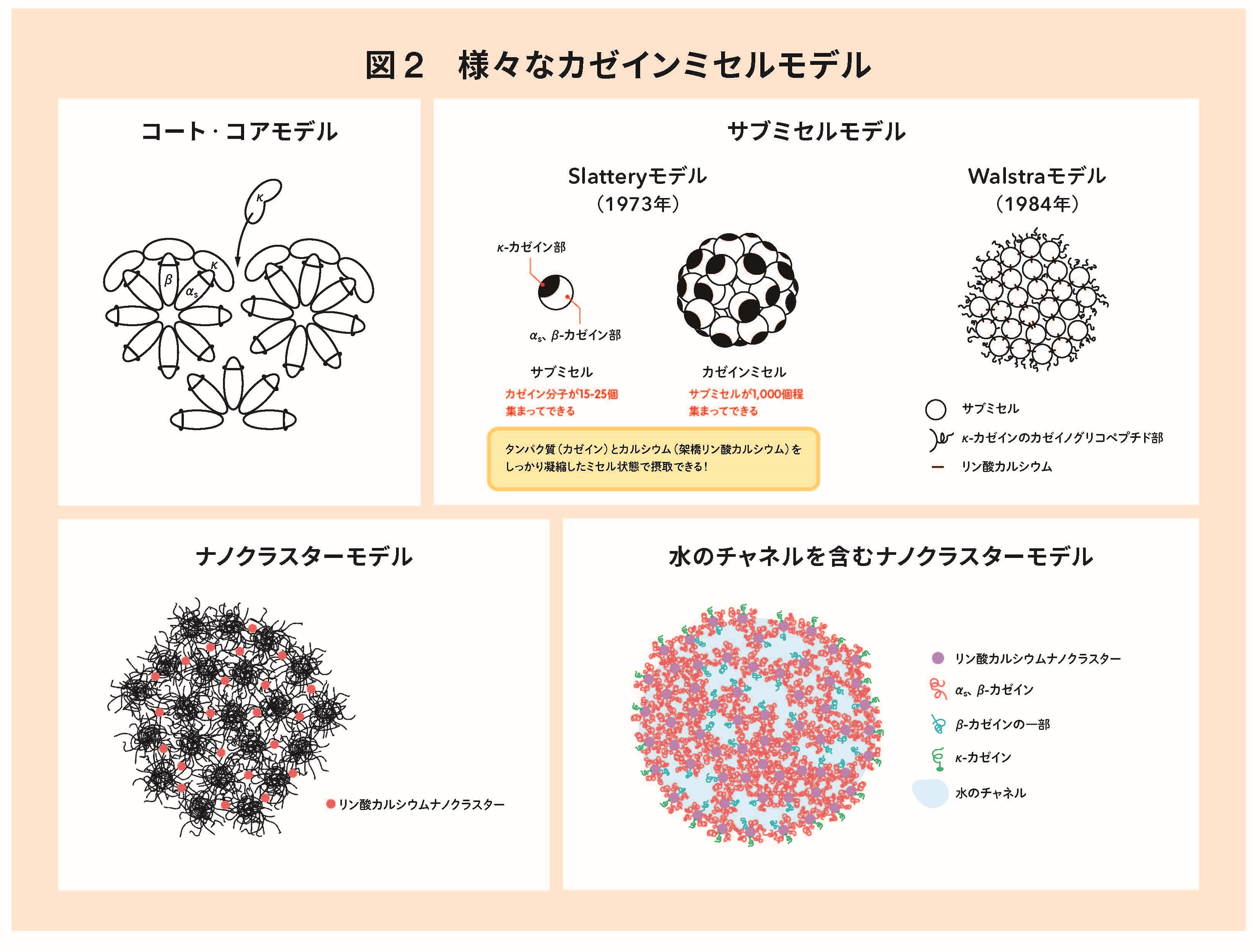
カゼインミセルの構造は、コロイド学の知見からコートコア説が提唱されました。続いて電子顕微鏡観察からいろいろな構造が提唱され、サブミセル構造説が、さらに化学的な研究や物理化学的な研究が加わり、ナノクラスター説が提案されています(図2)。
現時点ではナノクラスター説を支持する研究者が多数派となっています。最近では中性子光散乱やAIを利用した研究も行われています。しかしながら決定的な結論は未だ闇の中です。
筆者は常識に囚われており、重要な何かを見落としているのではないかと考えています。全ての哺乳類は仔の生命を維持し、発育させる目的で乳を出します。しかし、哺乳類以外でも(乳を出さなくても)仔の生命維持と発育を担う物質として卵があります。なので、卵と乳の比較も必要なのかもしれません。
牛以外の動物乳のカゼインミセルを考えてみることも必要だと考えます。動物によりカゼインの種類や一次構造(アミノ酸の配列)は異なっています。人乳にはαS2カゼインがなく、αS1カゼインも少量しかなく、その代わりβカゼインが主要カゼインとなっています。このため、カゼインミセルの大きさは牛乳のそれより小さくなっています。豚乳ではミセル性リン酸カルシウム(ミセル内部でカゼインに結合しているリン酸カルシウム)が多く、豚乳を冷却してもカゼインの遊離はわずかしかありません(Umeda, Milk Sci., 54: 23-28, 2005)。でもミセルを形成し水中で安定に分散しています。凝乳酵素を働かせると物理化学的な性質は異なりますが、凝固してカードを生成します。ミセルの大きさも動物により異なりますが、安定的に分散しています。なので、これら各種動物乳のカゼインミセルに関する研究が進展すれば、牛乳を含めたカゼインミセルの構造が明確になってくるのではないかと期待しています。
「乳科学 マルド博士のミルク語り」は毎月20日に更新しています。
ⒸNPO法人チーズプロフェッショナル協会
無断転載禁