何故、カゼインはカルシウムで沈殿するのか?
カゼインはカルシウムがなければ水によく溶け、安定に分散しています。しかし、カルシウムを加えるとたちどころに凝集し沈殿してきます。何故なのでしょうか?
この現象を説明する考え方として“カルシウム架橋”説があります。すなわち、カルシウムはプラス電荷を2個持っています。そのため、図1に示すようにカルシウムのプラス電荷とカゼインのマイナス電荷が結合し、カゼインとカゼインがカルシウムを介して結合するという考え方が“カルシウム架橋”説です。しかし、本当にそうなのでしょうか? 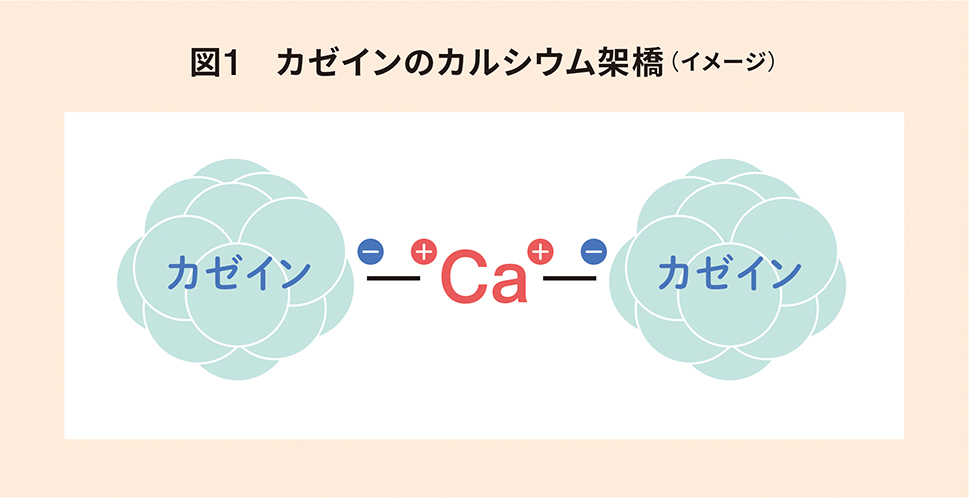
興味深い実験結果があります。カゼイン間でカルシウム架橋が働かないことを示す証拠を紹介します(Kaminogawa et al, J. Dairy Sci. 63:223-227, 1980)。カゼインにレンネットを作用させると真っ先にκ-CNが水との親和性の高いカゼインマクロペプチド(CMP)と親水性の低いパラκ-カゼインに分解します。しかし、チーズの熟成中に他のカゼインも分解しチーズの味や食感に大きな影響をもたらします。αs1-カゼインにレンネットが働くと、23個のアミノ酸からなるペプチド(仮に、N末ペプチドと呼びます)と残りの大きなペプチド(αs1-Ⅰ-CN)に分解されます。αs1-カゼインにカルシウムを加えるとたちまち沈殿しますが、レンネットを作用させてからカルシウムを加えても沈殿しません(図2)。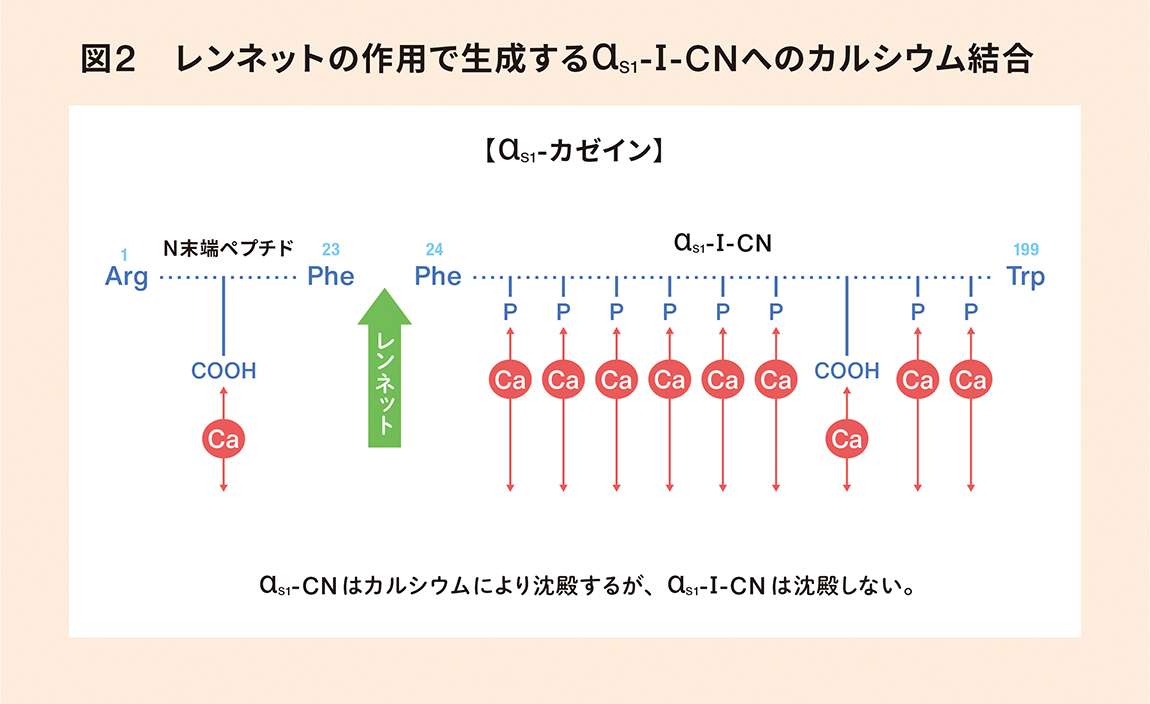
カルシウムはαs1-カゼインに含まれるリン酸が結合しているセリンというアミノ酸(Ser-P)のリン酸に最初に結合します。その後にアミノ酸のカルボキシル基(-COO)に結合します。全てのSer-Pはαs1-Ⅰ-CN部分に存在します。なので、カルシウムは真っ先にαs1-Ⅰ-CNのSer-Pに結合しますがαs1-Ⅰ-CNは沈殿しません。つまり、カルシウムがαs1-Ⅰ-CNに結合しても沈殿せず、カルシウム架橋は働いていないのです(図3)。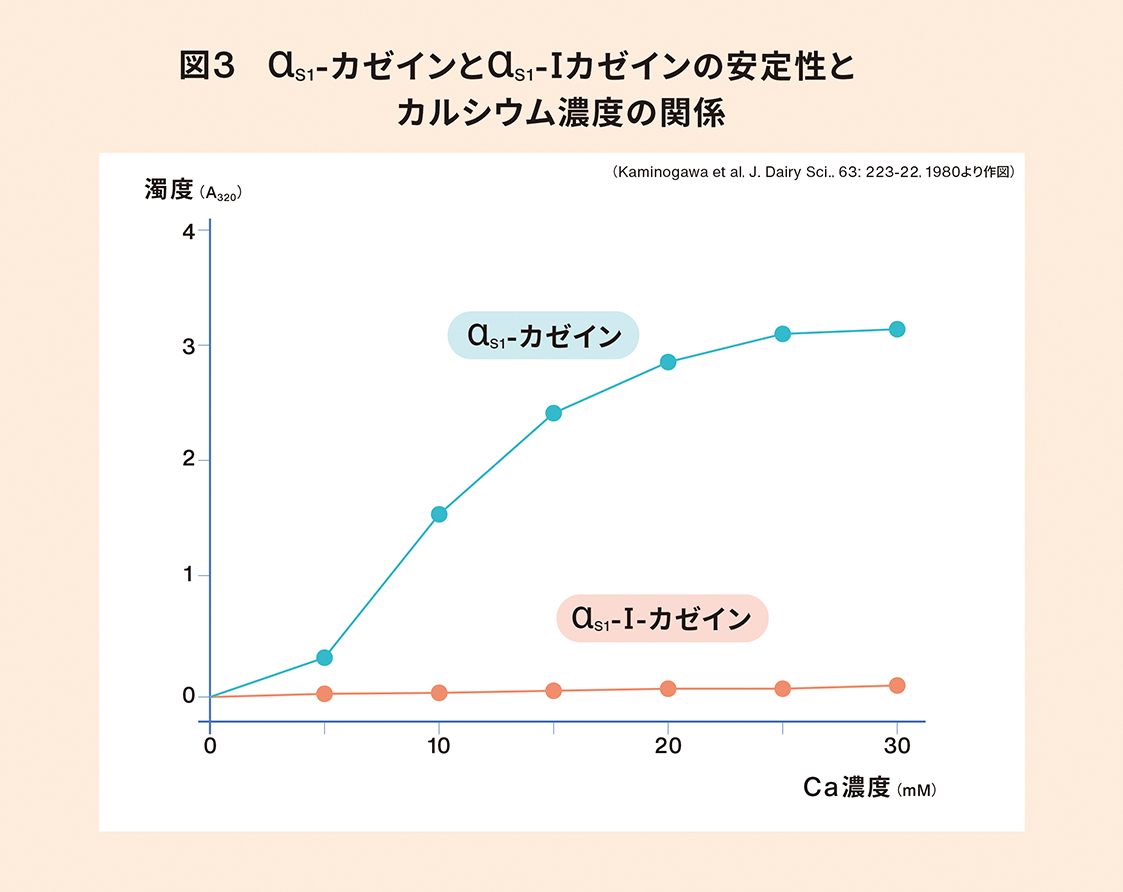
では、αs1-カゼインは何故カルシウムで沈殿するのでしょうか。実はまだ分かっていないのです。ただ、ヒントになるかもしれない現象があります。牛乳にレンネットを作用させるとカゼインミセルは凝集するのですが、カルシウムのない状態では凝集は起きません。エッ、と思う方が多いかもしれませんが、事実なのです。牛乳を超遠心分離機という装置で数万Gの遠心力でブンブン回転させるとカゼインミセルが沈殿してきます(Gは重力加速度。私たちは地上では1Gという重力を受けています。その数万倍の力をかけて1Gの重力で浮いているカゼインミセルを無理やり沈殿させます)。
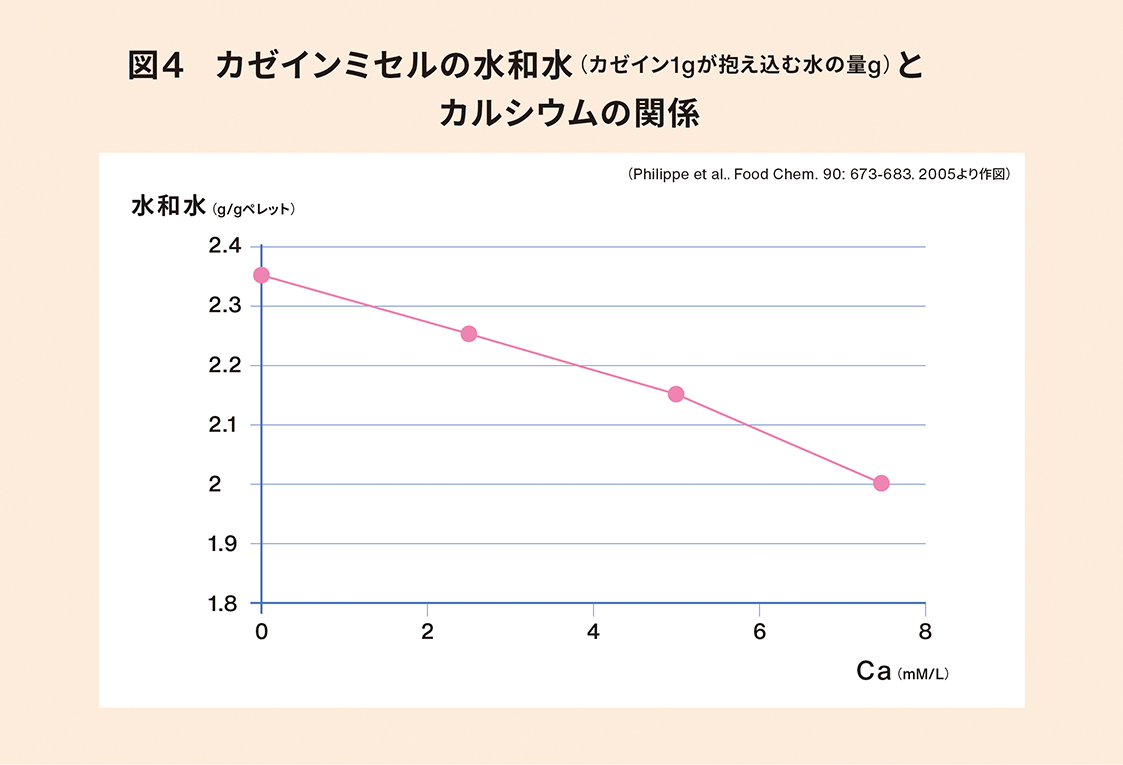
沈殿したカゼインミセルをカルシウムのない系に分散させレンネットを作用させると、κ-カゼインからCMPが遊離してくるのですが、凝集は起こりません。カゼインミセルにカルシウムを加えると水和量(CMが保持する水の量)が減少し、カルシウムを抜いていくと水和量が増えます(図4)。
つまり、カゼインミセルはカルシウムがないと水を大量に抱き込み、カルシウムがあると水を吐き出すのです。恐らく、カゼインミセルの表面にカルシウムが結合すると収縮し水を吐き出すと考えられます。同様の現象がαs1-カゼインでも起こっているのではないかと個人的には考えていますが、何故カルシウムで沈殿するのかを考えるには実験データが不十分です。さらなる研究が進展することを願っています。
「乳科学 マルド博士のミルク語り」は毎月20日に更新しています。
ⒸNPO法人チーズプロフェッショナル協会
無断転載禁止

